10. 化学小组以${NaOH}$为例,从定性和定量两个维度研究物质及其变化。
维度一:定性认识${NaOH}$及其溶液
(1)${NaOH}$属于“酸”或“碱”中的
碱
。
(2)将${NaOH}$曝露在空气中,可观察到表面潮湿并逐渐溶解。该现象反映出${NaOH}$的性质有
易潮解(合理即可)
(答一条)。
(3)向稀${NaOH}$溶液中滴加酚酞溶液,振荡,可观察到溶液由无色变为
红
色。
维度二:定量研究${NaOH}$溶液与不同物质的反应
Ⅰ. 酸碱度视角
25℃时,利用装置(图甲)测定${NaOH}$溶液与稀盐酸反应过程中pH的变化,测定结果如图乙所示(控制反应过程中温度不变)。
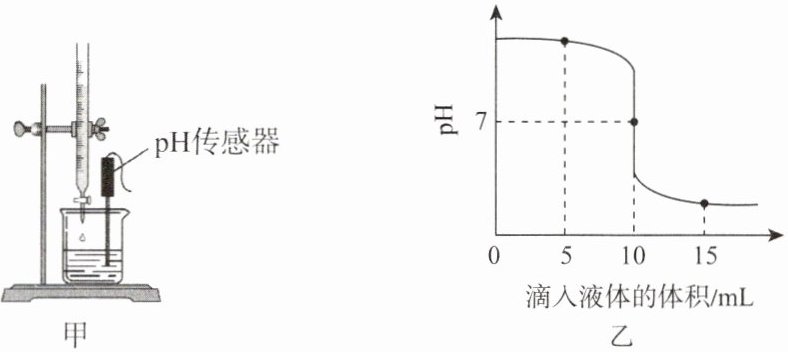
(4)烧杯中预先盛装的溶液是
氢氧化钠溶液
。
(5)当滴入液体的体积为
10
mL时,烧杯内溶液中的溶质只有${NaCl}$。
Ⅱ. 能量视角
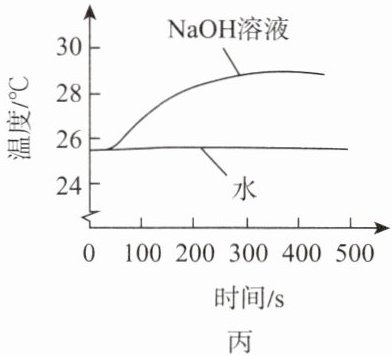
(6)利用传感器测定${NaOH}$溶液与${CO_{2}}$反应过程中温度的变化,测定结果如图丙所示,水为对照组。由图丙可知,${NaOH}$与${CO_{2}}$的反应属于
放热反应
(填“放热反应”或“吸热反应”)。
Ⅲ. 压强视角
[提出问题] 如何通过气体压强变化认识${NaOH}$溶液与${CO_{2}}$的反应?
[查阅资料]
① 可以通过反应物的减少或生成物的增加判断反应的发生情况;
② 影响密闭体系内气体压强的因素有气体分子数、气体所占体积和温度。
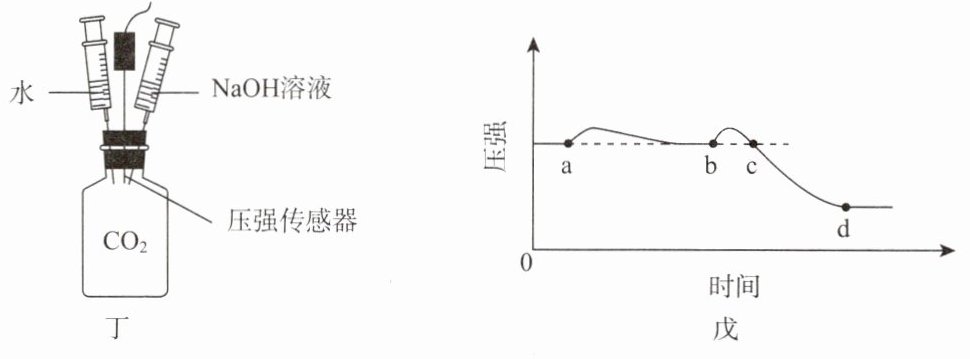
[实施实验] 利用气密性良好的装置(图丁)进行实验。打开压强传感器,待示数平稳后将水匀速注入充满${CO_{2}}$的集气瓶中,压强稳定后再匀速注入等体积的${NaOH}$溶液。测得气体压强变化如图戊所示。
[分析并解释数据]
(7)对比a点、b点及
d
点压强的大小,可证明${NaOH}$与${CO_{2}}$发生了反应。
(8)结合b→c的变化过程,解释b点、c点压强相同的原因:
在b→c的变化过程中:注入$\mathrm{NaOH}$溶液,气体所占体积减小,压强增大;$\mathrm{CO}_2$与$\mathrm{NaOH}$溶液反应放热,温度升高,压强增大;$\mathrm{CO}_2$与$\mathrm{NaOH}$溶液反应,$\mathrm{CO}_2$分子数减少,压强减小。各种因素的影响相互抵消,b点与c点的压强相同。(合理即可)
。