1. 地球上的金属资源广泛地存在于
地壳
和
海洋
中,除了
金
、
银
等有
单质
形式存在,金属多以
化合物
的形式存在。
答案:1. 地壳 海洋 金 银 单质 化合物
2. 把铁矿石冶炼成铁是一个复杂的过程,主要反应原理是在
高温
下,利用
高炉内反应生成的一氧化碳
把铁从氧化铁里
还原
出来,其反应的化学方程式为
$\mathrm{Fe_2O_3 + 3CO \overset{高温}{=} 2Fe + 3CO_2}$
。
答案:2. 高温 高炉内反应生成的一氧化碳 还原 $\mathrm{Fe_2O_3 + 3CO \overset{高温}{=} 2Fe + 3CO_2}$
3. 铁锈的主要成分为
氧化铁(或$\mathrm{Fe_2O_3 · xH_2O}$)
。如果隔绝了
空气或水
,就能在一定程度上防止铁生锈。在铁制品表面
涂油
、
刷漆
、
镀耐磨和耐腐蚀的铬
,以及
制造耐腐蚀的合金(答案合理即可)
等,都能防止铁制品锈蚀。
答案:3. 氧化铁(或$\mathrm{Fe_2O_3 · xH_2O}$) 空气或水 涂油 刷漆 镀耐磨和耐腐蚀的铬 制造耐腐蚀的合金(答案合理即可)
4. 金属矿物的储量有限,而且不能再生,因此,必须保护金属资源。保护金属资源的有效途径有
防止金属腐蚀
、
回收利用废旧金属
、
合理开采金属矿物
,以及
寻找金属的代用品
等。
答案:4. 防止金属腐蚀 回收利用废旧金属 合理开采金属矿物 寻找金属的代用品
问题 1. 实验室如何模拟炼铁?工业上是如何炼铁的?
要点
1. 实验室一氧化碳还原氧化铁的装置。
2. 工业炼铁的主要设备是
高炉
,原料是
赤铁矿石
、
焦炭
、
石灰石
等。
应用
图 1 是模拟炼铁的实验装置,试回答:
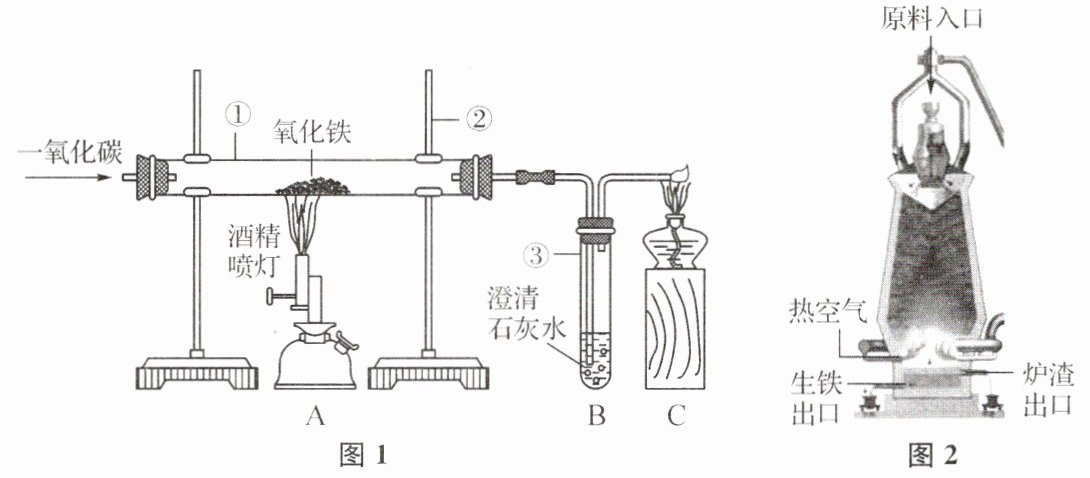
(1) 仪器①的名称是
硬质玻璃管(或玻璃管)
;仪器②的名称是
铁架台
。
(2) 实验过程中仪器①内发生反应的化学方程式是
$\mathrm{Fe_2O_3 + 3CO \overset{高温}{=} 2Fe + 3CO_2}$
,仪器③中的现象是
澄清石灰水变浑浊
。
(3) 实验过程中 C 处酒精灯的作用是
处理尾气,防止有毒的一氧化碳逸出污染空气
。
(4) 按图 1 连接实验装置、检查装置的气密性、装药品、固定实验装置后,主要实验步骤有:①通入一氧化碳;②停止通入一氧化碳;③点燃酒精喷灯;④熄灭酒精喷灯;⑤验纯。正确的操作顺序是
⑤①③④②
(填序号)。
(5) 图 2 是工业生产中高炉的结构图。实际生产中的原料从入口加入,其中焦炭在高炉中的作用之一是产生高温,另一个作用为
和$\mathrm{CO_2}$反应生成$\mathrm{CO}$作还原剂
;生铁出口低于炉渣出口的原因是
炉渣的密度小于生铁的密度
。
(6) 取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是
固体部分溶解,产生气泡,溶液由无色变为浅绿色
,发生反应的化学方程式为
$\mathrm{Fe + 2HCl = FeCl_2 + H_2 \uparrow}$
。当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质主要是
C
(填化学式)。
答案:问题1 要点:2 高炉 赤铁矿石 焦炭 石灰石 应用:(1)硬质玻璃管(或玻璃管) 铁架台 (2)$\mathrm{Fe_2O_3 + 3CO \overset{高温}{=} 2Fe + 3CO_2}$ 澄清石灰水变浑浊 (3)处理尾气,防止有毒的一氧化碳逸出污染空气 (4)⑤①③④② (5)和$\mathrm{CO_2}$反应生成$\mathrm{CO}$作还原剂 炉渣的密度小于生铁的密度 (6)固体部分溶解,产生气泡,溶液由无色变为浅绿色 $\mathrm{Fe + 2HCl = FeCl_2 + H_2 \uparrow}$ C