15. (6分)天然气(主要成分为$CH_4)$可用于制备碳材料和高纯$H_2,$其流程如图。请回答下列问题:
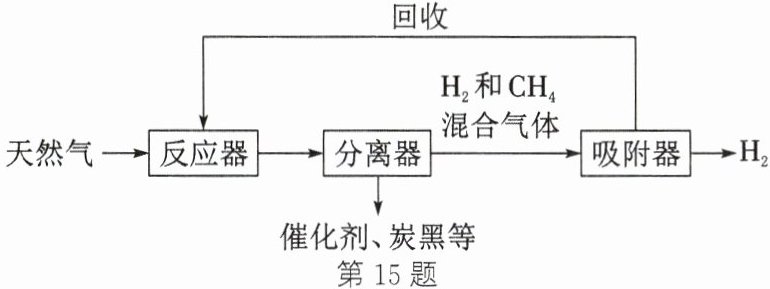
(1)“反应器”中,高温催化分解天然气可生成C和$H_2,$该反应的化学方程式为______
${CH_{4}\xlongequal[高温]{催化剂}C + 2H_{2}}$
。
(2)流程中,可回收利用的气体是______
${CH_{4}}$
。
(3)“积碳”:制备过程中,催化剂表面堆积较多的含碳物质。“积碳”会降低反应速率,其本质原因是______
含碳物质隔开了甲烷和催化剂
。
(4)“消碳”:除去催化剂表面堆积的含碳物质。高温时,将“积碳”的催化剂置于$CO_2$气流中可除去C,生成CO气体,该反应的化学方程式为______
${CO_{2} + C\xlongequal{高温}2CO}$
,属于______
化合反应
(填基本反应类型)。
(5)不同催化剂的相关参数如下表,分析可知,最合适的催化剂为______
a
(填序号)。
|催化剂序号|最佳反应温度/℃|最佳反应温度下的使用寿命/h|积碳量/mg|
|a|500|90|250|
|b|600|80|585|
|c|760|2|19|
答案:(1)${CH_{4}\xlongequal[高温]{催化剂}C + 2H_{2}}$ (2)${CH_{4}}$ (3)含碳物质隔开了甲烷和催化剂 (4)${CO_{2} + C\xlongequal{高温}2CO}$ 化合反应 (5)a 解析:(1)天然气的主要成分是甲烷,甲烷在高温和催化剂作用下生成碳和氢气,反应的化学方程式为${CH_{4}\xlongequal[高温]{催化剂}C + 2H_{2}}$。(2)分析该流程图可知,该流程中,可回收利用的气体是${CH_{4}}$。(3)“积碳”会降低反应速率,是因为含碳物质隔开了甲烷和催化剂。(4)二氧化碳和碳在高温条件下反应生成一氧化碳,反应的化学方程式为${CO_{2} + C\xlongequal{高温}2CO}$,该反应符合“多变一”的特征,属于化合反应。(5)分析表中数据可知,催化剂a的最佳反应温度最低,最佳反应温度下的使用寿命最长,积碳量适中,是最合适的催化剂。
解析:
(1)$CH_{4}\xlongequal[高温]{催化剂}C + 2H_{2}$
(2)$CH_{4}$
(3)含碳物质隔开了甲烷和催化剂
(4)$CO_{2} + C\xlongequal{高温}2CO$;化合反应
(5)a
16. (6分)实验室有一包铁粉和铜粉的混合物,现取该混合物10g于烧杯中,进行如下实验。请根据图中的实验过程及数据进行计算。(提示:铜与稀硫酸不反应,铁与稀硫酸反应的化学方程式为$Fe+H_2SO_4= FeSO_4+H_2↑)$
(1)混合物中铁粉的质量为
5.6g
。
(2)反应生成氢气的质量为
0.2g
。
(3)稀硫酸中溶质的质量分数是多少?(写出计算过程)
解:设恰好完全反应时,消耗${H_{2}SO_{4}}$的质量为x。
${Fe + H_{2}SO_{4}\xlongequal{}FeSO_{4} + H_{2}\uparrow }$
56 98
5.6g x
$\dfrac{56}{98}=\dfrac{5.6\mathrm{g}}{x}$ $x=9.8\mathrm{g}$
稀硫酸中溶质的质量分数为$\dfrac{9.8\mathrm{g}}{49\mathrm{g}}× 100\%=20\%$。
答:稀硫酸中溶质的质量分数为20%。
答案:(1)5.6g (2)0.2g (3)解:设恰好完全反应时,消耗${H_{2}SO_{4}}$的质量为x。
${Fe + H_{2}SO_{4}\xlongequal{}FeSO_{4} + H_{2}\uparrow }$
56 98
5.6g x
$\dfrac{56}{98}=\dfrac{5.6\mathrm{g}}{x}$ $x=9.8\mathrm{g}$
稀硫酸中溶质的质量分数为$\dfrac{9.8\mathrm{g}}{49\mathrm{g}}× 100\%=20\%$。
答:稀硫酸中溶质的质量分数为20%。