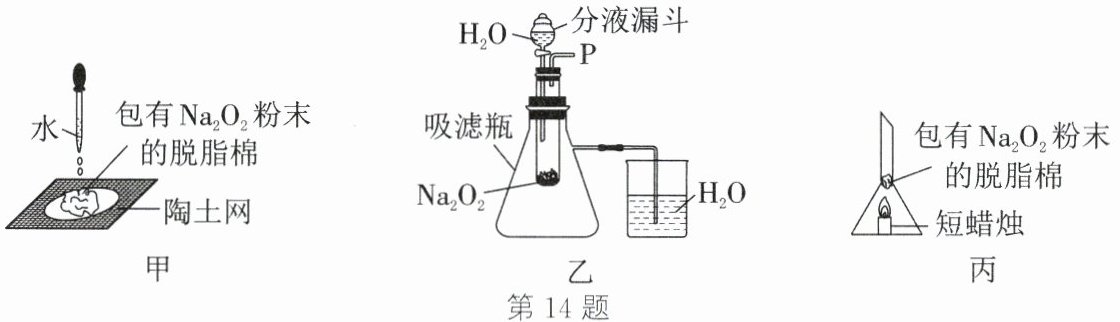
14. (8分)化学老师给同学们表演了一个“水能生火”的魔术(如图甲),他将包有过氧化钠$(Na_2O_2)$粉末的脱脂棉放在陶土网上,向脱脂棉上滴了几滴水,脱脂棉立刻燃烧起来。同学们对此产生了浓厚的兴趣,为什么脱脂棉会燃烧起来呢?
【提出猜想】
a. 小新认为过氧化钠与水反应生成了可支持燃烧的物质。
b. 小海又根据燃烧的条件,对小新的猜想进行了补充:
此反应还会放热
。
【实验分析】同学们设计了如图乙所示的实验装置。
(1) 打开分液漏斗的活塞,控制水滴加的速度,看到试管中有气泡产生,将带火星的木条靠近导管口P,看到木条复燃,你推测此气体可能是
氧气(或 O₂)
。
(2) 实验中还观察到烧杯中的导管口有气泡冒出,产生这一现象的原因是
过氧化钠与水反应放热,使吸滤瓶内压强增大
。
(3) 完成了以上实验,同学们继续探究反应后生成的另一种物质是什么。小新猜想另一种物质是$Na_2CO_3,$小海认为不可能,小海的依据是
反应物中没有碳元素
,通过进一步实验证明生成的另一种物质为氢氧化钠,写出发生反应的化学方程式:
2Na₂O₂ + 2H₂O = 4NaOH + O₂↑
。
【老师介绍】过氧化钠不仅可以和水发生反应,还可以和二氧化碳反应生成氧气,因此,过氧化钠经常被用于潜水艇和防毒面具中提供氧气。
【补充实验】明确了以上性质,小红又设计了一个实验(如图丙):将一团包有过氧化钠粉末的脱脂棉塞到漏斗的管中,漏斗口下方点燃一支短蜡烛(蜡烛火焰与脱脂棉不接触),则脱脂棉
能
燃烧。这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质:
水和二氧化碳
,同时反应放热。
【实验反思】结合实验,同学们对于运输过氧化钠固体提出了安全建议:
隔绝空气(或隔绝水;或密封保存等合理答案均可)
。