5. (2024·陕西)学习小组用一瓶长久放置、标签标示溶质质量分数为5%的过氧化氢溶液制取氧气,并用如图所示方法测定实验产生氧气的质量。请完成下列分析及计算:
(1)二氧化锰在反应前后的质量
不变
(填“变大”“变小”或“不变”)。
(2)实验产生氧气的质量是
1.6
g。
(3)通过计算说明实验所用过氧化氢溶液的溶质质量分数与标签标示的5%是否一致。
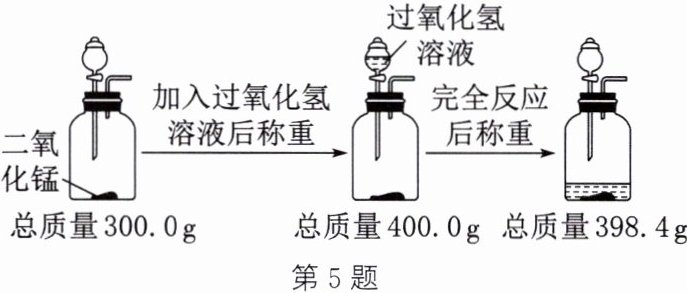
解:由图示可知,加入过氧化氢溶液的质量为$400.0\ \text{g} - 300.0\ \text{g} = 100.0\ \text{g}$。设生成$1.6\ \text{g}$氧气需要过氧化氢的质量为$x$。
${2H_{2}O_{2} \xlongequal{MnO_{2}} 2H_{2}O + O_{2} \uparrow}$
$\begin{array}{ccc}68 & 32 \\x & 1.6\ \text{g}\end{array}$
$\frac{68}{32} = \frac{x}{1.6\ \text{g}}\quad x = 3.4\ \text{g}$
所用过氧化氢溶液的溶质质量分数为$\frac{3.4\ \text{g}}{100.0\ \text{g}} × 100\% = 3.4\%$。
答:所用过氧化氢溶液的溶质质量分数与标签标示的$5\%$不一致。
答案:(1) 不变 (2) $1.6$ (3) 解:由图示可知,加入过氧化氢溶液的质量为$400.0\ \text{g} - 300.0\ \text{g} = 100.0\ \text{g}$。设生成$1.6\ \text{g}$氧气需要过氧化氢的质量为$x$。
${2H_{2}O_{2} \xlongequal{MnO_{2}} 2H_{2}O + O_{2} \uparrow}$
$\begin{array}{ccc}68 & 32 \\x & 1.6\ \text{g}\end{array}$
$\frac{68}{32} = \frac{x}{1.6\ \text{g}}\quad x = 3.4\ \text{g}$
所用过氧化氢溶液的溶质质量分数为$\frac{3.4\ \text{g}}{100.0\ \text{g}} × 100\% = 3.4\%$。
答:所用过氧化氢溶液的溶质质量分数与标签标示的$5\%$不一致。
6. (2024·兰州)兴趣小组同学得知鸡蛋壳的主要成分是碳酸钙,就用它来测定某瓶标签破损的稀盐酸中溶质的质量分数。称取5.5g干燥的鸡蛋壳(杂质不参加反应)于烧杯中,再将75g该稀盐酸分3次加入,充分反应后得到实验数据如表(已知:$CaCO_{3} + 2HCl = CaCl_{2} + H_{2}O + CO_{2}\uparrow$):
(1)鸡蛋壳中碳酸钙的质量为______g。
(2)求该稀盐酸中溶质的质量分数。(结果精确到0.1%)
|实验次序|第一次|第二次|第三次|
|稀盐酸的质量/g|25|25|25|
|剩余固体的质量/g|3|0.5|0.5|
(1)鸡蛋壳中碳酸钙的质量为
5
g。
(2)
解:由表格数据分析可知,$25\ \text{g}$稀盐酸与$2.5\ \text{g}$碳酸钙恰好完全反应。设$25\ \text{g}$稀盐酸中溶质的质量为$x$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
$\begin{array}{ccc}100 & 73 \\2.5\ \text{g} & x\end{array}$
$\frac{100}{73} = \frac{2.5\ \text{g}}{x}\quad x = 1.825\ \text{g}$
该稀盐酸中溶质的质量分数为$\frac{1.825\ \text{g}}{25\ \text{g}} × 100\% = 7.3\%$。
答:该稀盐酸中溶质的质量分数为$7.3\%$。
答案:(1) $5$ (2) 解:由表格数据分析可知,$25\ \text{g}$稀盐酸与$2.5\ \text{g}$碳酸钙恰好完全反应。设$25\ \text{g}$稀盐酸中溶质的质量为$x$。
${CaCO_{3} + 2HCl \xlongequal{} CaCl_{2} + H_{2}O + CO_{2} \uparrow}$
$\begin{array}{ccc}100 & 73 \\2.5\ \text{g} & x\end{array}$
$\frac{100}{73} = \frac{2.5\ \text{g}}{x}\quad x = 1.825\ \text{g}$
该稀盐酸中溶质的质量分数为$\frac{1.825\ \text{g}}{25\ \text{g}} × 100\% = 7.3\%$。
答:该稀盐酸中溶质的质量分数为$7.3\%$。
7. (2023·龙东地区)有碳酸镁和氢氧化镁的混合物10g,经测定,混合物中镁元素的质量分数为36%,向其中加入100g溶质质量分数为14.7%的稀硫酸,恰好完全反应得到不饱和溶液,将溶液蒸干后得到的固体质量为[已知:$MgCO_{3} + H_{2}SO_{4} = MgSO_{4} + CO_{2}\uparrow + H_{2}O,Mg(OH)_{2} + H_{2}SO_{4} = MgSO_{4} + 2H_{2}O$] (
B
)
A.12g
B.18g
C.24g
D.36g
答案:B 解析:有碳酸镁和氢氧化镁的混合物$10\ \text{g}$,经测定,混合物中镁元素的质量分数为$36\%$,则混合物中含有镁元素的质量为$10\ \text{g} × 36\% = 3.6\ \text{g}$。向其中加入$100\ \text{g}$溶质质量分数为$14.7\%$的稀硫酸,碳酸镁和稀硫酸反应生成硫酸镁、水和二氧化碳,氢氧化镁和稀硫酸反应生成硫酸镁和水,恰好完全反应时,将溶液蒸干后得到的固体为硫酸镁,反应前后镁元素的质量不变,则得到的固体质量为$\frac{3.6\ \text{g}}{\frac{24}{24 + 32 + 16 × 4} × 100\%} = 18\ \text{g}$。故本题选B。
8. (2023·齐齐哈尔)现有碳酸钠和氯化钠的固体混合物10.9g,加入93.5g水,固体完全溶解,向该溶液中加入稀盐酸,所得溶液质量与加入稀盐酸质量的关系如图所示(已知:$Na_{2}CO_{3} + 2HCl = 2NaCl + H_{2}O + CO_{2}\uparrow$)。请计算:
(1)恰好完全反应时,生成二氧化碳的质量是
4.4
g。
(2)恰好完全反应时,所得溶液中溶质的质量分数。(写出计算过程)

解:设生成氯化钠的质量为$x$,原固体混合物中碳酸钠的质量为$y$。
${Na_{2}CO_{3} + 2HCl \xlongequal{} 2NaCl + H_{2}O + CO_{2} \uparrow}$
$\begin{array}{ccc}106 & 117 & 44 \\y & x & 4.4\ \text{g}\end{array}$
$\frac{117}{44} = \frac{x}{4.4\ \text{g}}\quad x = 11.7\ \text{g}$
$\frac{106}{44} = \frac{y}{4.4\ \text{g}}\quad y = 10.6\ \text{g}$
恰好完全反应时,所得溶液中溶质的质量分数为$\frac{11.7\ \text{g} + 10.9\ \text{g} - 10.6\ \text{g}}{200\ \text{g}} × 100\% = 6\%$。
答:恰好完全反应时,所得溶液中溶质的质量分数为$6\%$。
答案:(1) $4.4$ (2) 解:设生成氯化钠的质量为$x$,原固体混合物中碳酸钠的质量为$y$。
${Na_{2}CO_{3} + 2HCl \xlongequal{} 2NaCl + H_{2}O + CO_{2} \uparrow}$
$\begin{array}{ccc}106 & 117 & 44 \\y & x & 4.4\ \text{g}\end{array}$
$\frac{117}{44} = \frac{x}{4.4\ \text{g}}\quad x = 11.7\ \text{g}$
$\frac{106}{44} = \frac{y}{4.4\ \text{g}}\quad y = 10.6\ \text{g}$
恰好完全反应时,所得溶液中溶质的质量分数为$\frac{11.7\ \text{g} + 10.9\ \text{g} - 10.6\ \text{g}}{200\ \text{g}} × 100\% = 6\%$。
答:恰好完全反应时,所得溶液中溶质的质量分数为$6\%$。
解析:(1) 由质量守恒定律可知,生成二氧化碳的质量为$10.9\ \text{g} + 93.5\ \text{g} + 100\ \text{g} - 200\ \text{g} = 4.4\ \text{g}$。