13. 人体缺乏维生素 C(简称 VC)易患坏血病。如图是盛放“维生素 C”瓶子标签的一部分,根据图中的信息回答下列问题。
(1) 维生素 C 中氢、氧两种元素的质量比为
1:12
(填最简整数比)。
(2) CₙH₈O₆ 中 n=
6
。
(3) 44 g 维生素 C 中含有氧元素的质量为
24g
。
(4) 维生素 C 中碳元素的质量分数是
40.9%
(结果精确到 0.1%)。
答案:(1) $1:12$ (2) 6 (3) $24g$ (4) $40.9\%$ 解析:(1) 维生素 C 中氢、氧两种元素的质量比为 $(1×8):(16×6) = 1:12$。(2) 维生素 C 的化学式量为 $12× n + 1×8 + 16×6 = 176$,解得 $n = 6$。(3) $44g$ 维生素 C 中含有氧元素的质量为 $44g×(\frac{16×6}{176}×100\%) = 24g$。(4) 维生素 C 中碳元素的质量分数为 $\frac{12×6}{176}×100\%\approx40.9\%$。
解析:
(1) 维生素C中氢、氧两种元素的质量比为$(1×8):(16×6)=8:96=1:12$。
(2) 由化学式量为176可得:$12n + 1×8 + 16×6=176$,$12n + 8 + 96=176$,$12n=72$,解得$n=6$。
(3) 44g维生素C中氧元素的质量为$44g×\frac{16×6}{176}=44g×\frac{96}{176}=24g$。
(4) 维生素C中碳元素的质量分数为$\frac{12×6}{176}×100\%=\frac{72}{176}×100\%\approx40.9\%$。
(1)1:12
(2)6
(3)24g
(4)40.9%
14. (2024·扬州宝应期中)关于分子、原子,下列说法正确的是 (
B
)
A.分子间有间隔,原子间没有间隔
B.化学变化前后原子的个数不变
C.原子不能直接构成物质
D.化学变化前后分子的种类不变
答案:B
15. (2024·苏州工业园区期中)下列化学用语书写正确的是 (
A
)
A.氨气:He
B.银元素:AG
C.2 个镁离子$:2Mg⁺^2$
D.8 个硫原子$:S_8$
答案:A
16. 下列对化学用语中“2”所表示意义的理解,正确的是 (
C
)
A.2Mg 中的“2”表示 2 个镁元素
$B.H_2 $中的“2”表示 2 个氢原子
$C.2Fe^3⁺ $中的“2”表示 2 个铁离子
D.$\overset{+2}{\text{Cu}}$O 中的“2”表示铜原子的化合价为+2
答案:C
解析:
A.元素只讲种类,不讲个数,2Mg中的“2”表示2个镁原子,A错误;
B.H₂中的“2”表示1个氢分子中含有2个氢原子,B错误;
C.2Fe³⁺中的“2”表示2个铁离子,C正确;
D.$\overset{+2}{\text{Cu}}$O中的“2”表示氧化铜中铜元素的化合价为+2,D错误。
答案:C
17. (2025·宿迁宿豫期末)对下面符号或示意图的认识,正确的是 (
A
)
$A. NaNO_3 $中氮元素的化合价是+5
$B. Fe^2⁺、$$Fe^3⁺ $都属于铁元素,是同一种离子
$C. NO_2、$$N_2O_4 $中氮元素的化合价都是+4,是同一种化合物
D.
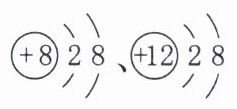
两种微观粒子的核外电子排布情况相同,属于同一种元素
答案:A
解析:
解:A选项:在$NaNO_3$中,钠元素显+1价,氧元素显-2价,设氮元素的化合价为$x$,根据化合物中正负化合价代数和为零,可得:$(+1)+x+(-2)×3=0$,解得$x=+5$,A正确。
B选项:$Fe^{2+}$、$Fe^{3+}$质子数相同,都属于铁元素,但核外电子数不同,是不同种离子,B错误。
C选项:$NO_2$、$N_2O_4$化学式不同,是不同种化合物,C错误。
D选项:核外电子排布相同的微观粒子,质子数不一定相同,不一定属于同一种元素,D错误。
答案:A
18. 如图是镉的原子结构示意图及其在元素周期表中的信息,则有关镉的说法不正确的是 (
D
)
A.镉原子在化学反应中易失去电子
B.镉元素符号为 Cd
C.镉原子的质子数为 48
D.镉属于非金属元素
答案:D
19. (2024·宿迁宿豫期中)荷叶中含有荷叶碱,荷叶碱有降血脂、抗自由基、抑制高胆固醇血症和动脉硬化等功效,其化学式为$ C_1_9H_2_1NO_2。$下列说法中,正确的是 (
C
)
A.荷叶碱中碳、氢两种元素的质量比为 19:21
B.荷叶碱是由 19 个碳原子、21 个氢原子、1 个氮原子和 2 个氧原子构成的
C.荷叶碱是由碳、氢、氮、氧四种元素组成的化合物
D.荷叶碱中氢元素的质量分数最大
答案:C
解析:
解:
A. 荷叶碱中碳、氢两种元素的原子个数比为19:21,质量比为(12×19):(1×21)=228:21=76:7,A错误;
B. 一个荷叶碱分子是由19个碳原子、21个氢原子、1个氮原子和2个氧原子构成的,B错误;
C. 荷叶碱是由碳、氢、氮、氧四种元素组成的化合物,C正确;
D. 荷叶碱中碳、氢、氮、氧元素的质量比为(12×19):(1×21):14:(16×2)=228:21:14:32,碳元素的质量分数最大,D错误。
结论:C
20. 羟基磷酸钙是人的牙齿中一种比较坚硬的物质,其化学式为$ Caₓ(PO_4)_6(OH)ᵧ($其中磷元素的化合价为+5)。经分析,其中钙、氧元素的质量比为 25:26,则 (
A
)
A.x:y= 5:1
B.x:y= 5:2
C.x:y= 5:3
D.x:y= 5:4
答案:A
解析:
解:在$Ca_x(PO_4)_6(OH)_y$中,磷元素显+5价,氧元素显-2价,氢元素显+1价,钙元素显+2价。
根据化合物中各元素正负化合价代数和为零,可得:$2x + 6×(+5) + y×(+1) + [4×6 + y]×(-2) = 0$,化简得$2x - y = 18$。
钙元素质量为$40x$,氧元素质量为$16×(24 + y)$,已知钙、氧元素质量比为25:26,即$\frac{40x}{16×(24 + y)} = \frac{25}{26}$,化简得$13x - 5y = 150$。
联立方程组$\begin{cases}2x - y = 18 \\13x - 5y = 150\end{cases}$,解得$x = 10$,$y = 2$,则$x:y = 10:2 = 5:1$。
答案:A
21. 在农业科研实验室里,可用一定量的$ NH_4NO_3 $和$ K_2SO_4 $的固体混合物配制无土栽培营养液。已知固体混合物中氮元素的质量分数为 14%,则固体混合物中$ K_2SO_4 $的质量分数为 (
D
)
A.85%
B.80%
C.65%
D.60%
答案:D 解析: $NH_{4}NO_{3}$ 中氮元素的质量分数为 $\frac{14×2}{14 + 1×4 + 14 + 16×3}×100\% = 35\%$,由于混合物中氮元素的质量分数为 $14\%$,因此硝酸铵在混合物中的质量分数为 $\frac{14\%}{35\%}×100\% = 40\%$,所以固体混合物中 $K_{2}SO_{4}$ 的质量分数为 $1 - 40\% = 60\%$,D 选项正确。