7. 用如图装置进行$CO_{2}$的制取、收集和验满实验,利用传感器和数据采集器测定$CO_{2}$的体积分数并观察木条的燃烧状况,记录如表(不考虑空气中原有$CO_{2}$及木条燃烧产生的气体对实验结果的影响)。下列说法错误的是 (
C
)
A.采用分液漏斗可以节约试剂、控制反应速率
B.若木条正常燃烧,则瓶内体积分数最大的气体是$N_{2}$
C.当$O_{2}$的体积分数为 20%时,瓶口的木条熄灭
D.该实验说明要收集较纯净的$CO_{2}$,需在木条熄灭后继续通入$CO_{2}$一段时间
答案:C 解析:采用分液漏斗可以节约试剂,还可以控制添加试剂的速度,进而控制反应速率,A 正确;若木条正常燃烧,此时装置内二氧化碳的体积分数为 36.3%,瓶中空气的体积分数为$1 - 36.3\% = 63.7\%$,则氮气的体积分数为$63.7\%×78\% ≈ 49.69\%$,所以此时瓶内氮气的体积分数最大,B 正确;木条熄灭时,装置中二氧化碳的体积分数为 44.3%,装置中空气的体积分数为$1 - 44.3\% = 55.7\%$,则氧气的体积分数为$55.7\%×21\% ≈ 11.70\%$,C 错误;木条熄灭时,装置内${CO_{2}}$的体积分数为 44.3%,因此要收集较纯净的${CO_{2}}$,需在木条熄灭后的一段时间内继续通入${CO_{2}}$,D 正确。故本题选 C。
8. 下列实验室制取二氧化碳的发生装置中,不能控制反应随时发生或停止的是 (
B
)
答案:B 解析:关闭止水夹,U 形管右侧压强增大,液体被压入漏斗中,固液分离;打开止水夹后,固液接触,反应进行,能控制反应随时发生或停止,A 正确。大理石放在锥形瓶中,加入稀盐酸后,酸和固体不能分离,不能控制反应随时发生或停止,B 错误。关闭止水夹,试管内压强增大,液体被压回长颈漏斗中,固液分离;打开止水夹后,固液接触,反应进行,能控制反应随时发生或停止,C 正确。可以通过抽动铜丝,上下移动铜网,控制大理石与稀盐酸的接触与分离,能控制反应随时发生或停止,D 正确。故本题选 B。
9. 实验小组在实验室里进行制取气体的实验探究。实验台上给的有高锰酸钾、过氧化氢溶液、二氧化锰、稀硫酸、石灰石和稀盐酸,以及如图所示仪器。
(1) 实验小组首先打算制取二氧化碳,小组成员应选择的仪器有
①②⑦⑧
(填序号),应选择的试剂是
石灰石和稀盐酸
。
(2) 若实验小组打算选用与(1)不同的试剂,但用与(1)相同的装置制取其他气体,请书写制取该气体的化学方程式:
${2H_{2}O_{2}\xlongequal{{MnO_{2}}}2H_{2}O + O_{2}\uparrow}$
。
(3) 在制取二氧化碳的实验过程中,长颈漏斗的末端要始终
伸入液面以下
,以防止气体从漏斗口逸出。
答案:(1)①②⑦⑧ 石灰石和稀盐酸 (2)${2H_{2}O_{2}\xlongequal{{MnO_{2}}}2H_{2}O + O_{2}\uparrow}$ (3)伸入液面以下
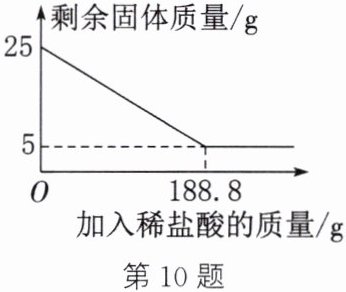
10. 实验室常用大理石和稀盐酸制取二氧化碳。现取 25 g 大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。
(1) 25 g 大理石中碳酸钙的质量为
20 g
。
(2) 求恰好完全反应时生成二氧化碳的质量。
(2)解:设恰好完全反应时生成二氧化碳的质量为$x$。
${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow}$
100 44
20 g $x$
$\dfrac{100}{44} = \dfrac{20\ {g}}{x}$
$x = 8.8\ {g}$
答:恰好完全反应时生成二氧化碳的质量为 8.8 g。
答案:(1)20 g (2)解:设恰好完全反应时生成二氧化碳的质量为$x$。${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow}$100 4420 g $x$$\dfrac{100}{44} = \dfrac{20\ {g}}{x}$ $x = 8.8\ {g}$答:恰好完全反应时生成二氧化碳的质量为 8.8 g。